Der nächste Lithium-Ionen-Akku ist immer nur einen Handgriff weit entfernt: Kein Smartphone kommt heute ohne jenen leistungsfähigen, kompakten und flexiblen Stromspeicher aus. Doch neben den nur wenige Kubikzentimeter großen Handyakkus lassen sich Lithium-Ionen-Batterien durch Parallel- und Serienschaltung von Zellen in nahezu jeder gewünschten Baugröße und Kapazität herstellen. Vor allem Elon Musk baut im großen Stil auf diese Technologie: Nicht nur der Tesla fährt mit Lithium-Ionen-Strom, Musk installierte Ende des vergangenen Jahres in Australien die derzeit weltgrößte Lithium-Ionen-Batterie. Seine in nur 63 Tagen erbaute 100-Megawatt-Einheit ist an einen Windpark angeschlossen und soll im Falle eines Stromausfalls 30.000 Haushalte bis zu eine Stunde lang mit Strom versorgen können. Auch das ist nur Vorgeplänkel: Tesla baut seit 2014 mit der Panasonic Corporation an der „Gigafactory 1“, einer Fabrik für Lithium-Ionen-Zellen und Batteriepakete, die ab 2018 etwa 500.000 Elektroautos jährlich mit bezahlbaren Stromspeichern versorgen will. Diese Fabrik soll die aktuellen Kosten für Lithium-Batterien um 30 Prozent senken. Ziel ist es, jährlich Zellen mit 35 Gigawattstunden Gesamtkapazität herstellen zu können. Das wäre mehr als die gesamte weltweite Produktion im Jahr 2013.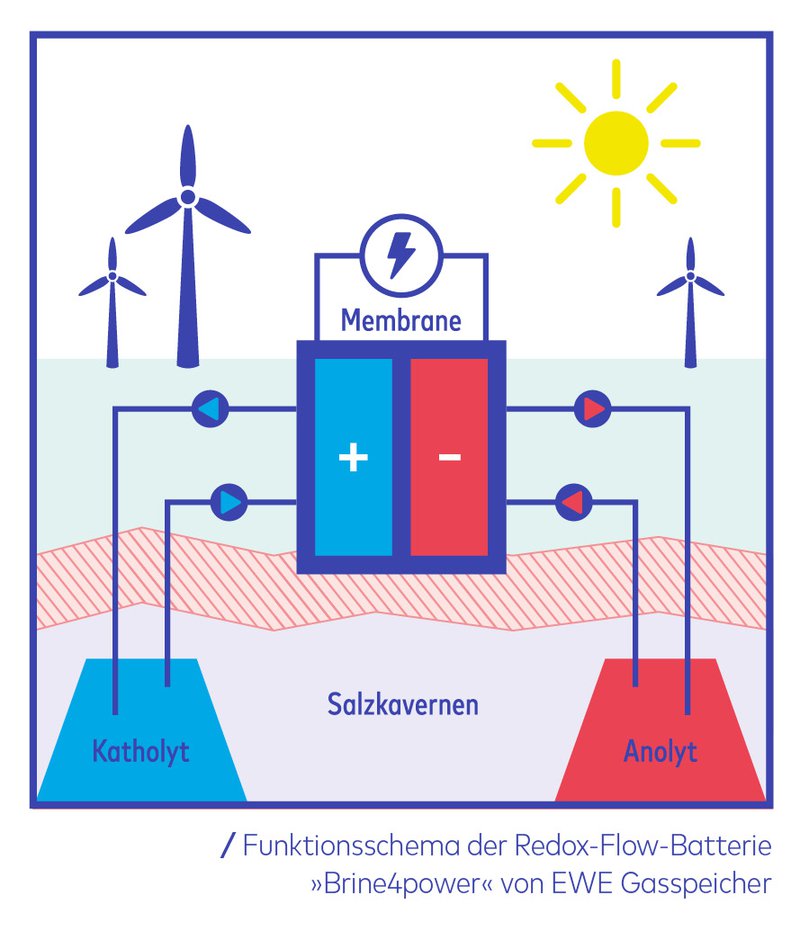
Gesucht: der ungefährliche, umweltfreundliche Akku
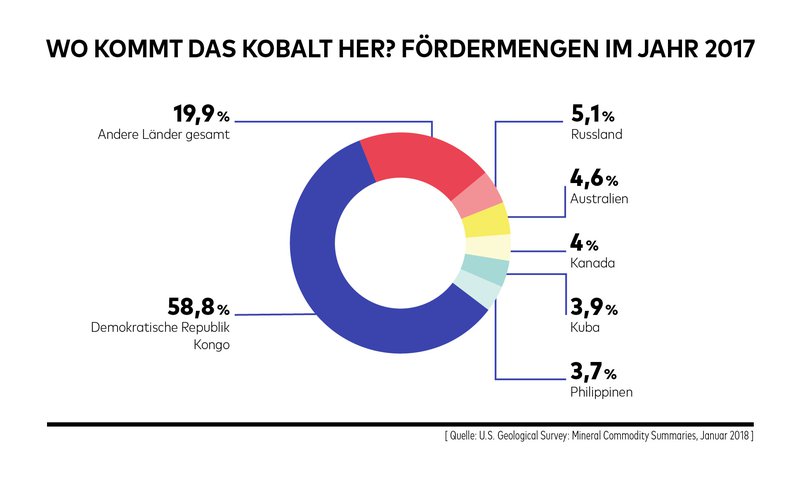
Solcherlei Pläne werden von Wissenschaftlern und Ökonomen mit einer gewissen Skepsis betrachtet – vor allem wegen der stetig steigenden Nachfrage nach dem Kathodenmaterial Kobalt. Dr. Peter Fischer vom Fraunhofer-Institut für Chemische Technologie (ICT) in Pfinztal forscht an alternativen Batteriekonzepten und sieht eine Fixierung auf Kobalt kritisch: „Das Material ist erstens weltweit nicht unbegrenzt verfügbar, außerdem wird es teilweise unter menschenunwürdigen Bedingungen und erheblichen Umweltbelastungen abgebaut. Und noch dazu in weit entfernten Ländern mit teilweise instabiler politischer Lage.“ So kamen im Jahr 2017 gut 58 Prozent, also deutlich mehr als die Hälfte des Rohstoffs, aus der Demokratischen Republik Kongo, danach folgen Russland, Australien und Kanada.
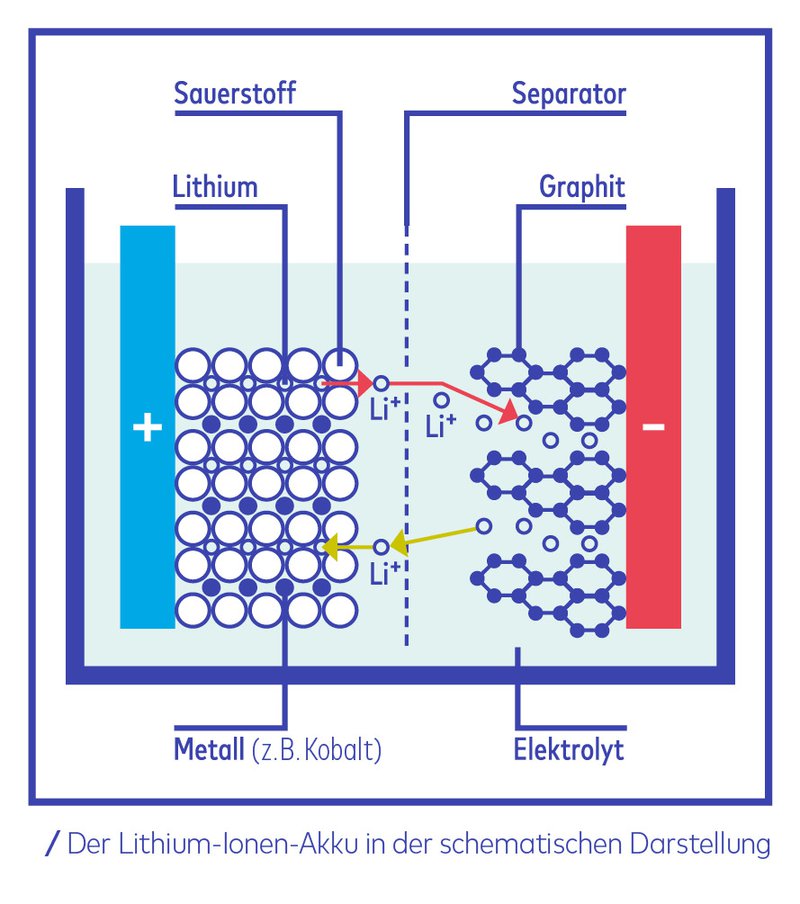
Auch technisch sei die Lithium-Ionen-Batterie trotz ihrer guten Performance nicht für alle Anwendungen der Zukunft die ideale Lösung: „Erstens ist ihre Zyklenzahl begrenzt, zweitens können Lithium-Batterien bei falscher Handhabung brennen und im schlimmsten Fall sogar zu Explosionen führen. Man hat die Gefahren heute zwar insgesamt ganz gut im Griff – es handelt sich dabei aber nicht per se um eine ungefährliche Technologie“, so Fischer. Die Brand- beziehungsweise Explosionsgefahr ist ein systemimmanenter Nachteil des verwendeten Elektrolyts, der aus einer brennbaren Flüssigkeit besteht, und des Lithiums, denn es ist in der Lage, sogenannte Dendriten zu bilden – sich tropfsteinartig ausbreitende Metallabscheidungen. Durch elektrochemische Vorgänge können auf den Elektroden von Lithium-Akkumulatoren solche Dendriten wachsen. Das geschieht vor allem, wenn ein solcher Akku zu schnell oder bei niedriger Temperatur geladen wird. Wenn es den Dendriten gelingt, den Separator zwischen den Elektroden zu durchdringen, kann dies zum Kurzschluss in der Zelle führen.
Peter Fischer nennt aber auch weitere Bedarfe für alternative Batterietechnologien, insbesondere wenn es um stationäre Speicher geht: Hier seien zum einen möglichst niedrige Herstellungskosten und zum anderen eine möglichst unendliche Lebensdauer gefragt – beides nicht gerade die Königsdisziplinen des Lithium-Ionen-Akkus. Es gibt also Gründe genug, nach Alternativen zu forschen. Derzeit konzentriert sich die Forschung primär auf zwei Zweige: zum einen auf das Grundprinzip des klassischen Akkumulators, bei dem jedoch statt Lithium andere Ionenquellen wie Natrium oder Magnesium eingesetzt werden, zum anderen auf die Redox-Flow-Batterie.
Die Mischung macht’s
Das Ulmer Helmholtz-Institut (HIU) gehört hierzulande zu den ersten Adressen, wenn es um Alternativen zum Lithium-Ionen-Akku geht. Die Wissenschaftler dieses Batterieforschungszentrums testen Batteriezellen mit unterschiedlichen Materialkombinationen und bestimmen deren Energiedichte, Leistung und Lebensdauer. Man möchte herausfinden, wie Elementarprozesse das Funktionieren von elektrochemischen Energiespeichern beeinflussen. Außerdem sollen elektrochemische Effekte durch die Verbindung von experimentellen Messungen mit Simulationen nachvollzogen werden, um Schlussfolgerungen für Anwendungen in der Praxis zu ziehen. Vielversprechende Ersatzkandidaten für Lithium sind laut Prof. Dr. Maximilian Fichtner vom HIU die Metalle Magnesium, Natrium und Aluminium – allesamt Materialien, die zwar derzeit noch nicht die Energiedichte eines Lithium-Ionen-Akkus erreichen, dafür aber in praktisch unbegrenzter Menge verfügbar sind. Doch auch der Lithium-Ionen-Akku kann noch verbessert werden: So hat die interdisziplinäre Forschungsgruppe um Fichtner gemeinsam mit Prof. Dr. Mario Ruben vom Institut für Nanotechnologie des Karlsruher Instituts für Technologie (KIT) im Spätsommer 2017 ein neues Speichermaterial vorgestellt, dass die sehr schnelle und reversible Einlagerung von Lithium-Ionen erlaubt. Dazu wurde ein organisches Molekül mit funktionellen Gruppen versehen, die beim ersten Beladungsvorgang in der Batteriezelle eine strukturelle und elektrisch leitende Vernetzung des Materials herbeiführen. Das stabilisiert die Struktur der Elektrode in hohem Maße und macht mehrere Tausend Lade- und Entladezyklen möglich. „Diese Speichereigenschaften sind außergewöhnlich, weil das Material eine Speicherkapazität wie ein Batteriematerial besitzt – aber so schnell arbeitet wie ein Superkondensator“, so Fichtner.
Alles im Flow?
Ein gänzlich anderes Prinzip wirkt in der Redox-Flow-Batterie. Sie speichert Energie in flüssigen chemischen Verbindungen. Notwendig für den Betrieb einer solchen Batterie sind zwei energiespeichernde Elektrolyte. Sie zirkulieren über Pumpen in getrennten Kreisläufen und werden dann in einer sogenannten galvanischen Zelle an Elektroden herangeführt: Dort findet die elektrochemische Reaktion statt. Eine Membran, die selektiv Ionen passieren lässt, verhindert ein Durchmischen der beiden Elektrolyte in der Zelle, erlaubt es aber, dass Ladungen fließen können. Sobald ein elektrischer Verbraucher an die beiden Batteriepole angeschlossen wird, findet in der Zelle eine elektrochemische Reaktion statt und die Elektrolytlösung wird entladen. Wird hingegen an den Polen eine Spannungsquelle angebracht, läuft die elektrochemische Reaktion in umgekehrter Richtung ab und die Elektrolytlösung wird neu aufgeladen. Ein zentraler Vorteil der Redox-Flow-Technik ist laut Dr. Peter Fischer vom Fraunhofer ICT die Langlebigkeit: „Theoretisch ist dieser Batterietyp unsterblich. Die Elektroden verändern sich – anders als beim Lithium-Ionen-Akku – während der elektrochemischen Reaktion nicht.“ Im Rahmen des Projekts „RedoxWind“ wird am Fraunhofer-Institut derzeit ein Redox-Flow-Großbatteriespeicher entwickelt, der direkt an den Gleichstromzwischenkreis einer Windenergieanlage gekoppelt wird. Das Projekt soll zeigen, ob es möglich ist, Dörfer, Kleinstädte oder Unternehmen auch ohne Anschluss an große Energienetze sicher mit Strom zu versorgen, indem sie eigenständig Energie produzieren und in eigenen Großbatterien speichern.
Salzwasser statt Schwefelsäure
Intensiv geforscht wird auch an der Friedrich-Schiller-Universität in Jena. Sie hat gemeinsam mit dem Zentrum für Energie und Umweltchemie (CEEC Jena) und der Jena-Batteries GmbH – einer Ausgründung der Uni Jena – eine Redox-Flow-Batterie auf Basis von Polymeren und einer Kochsalzlösung entwickelt. Dr. Martin Hager von der Universität Jena: „Das Neuartige an unserem Batteriesystem ist, dass es deutlich günstiger hergestellt werden kann, aber dennoch fast die Kapazität und Leistung herkömmlicher metall- und säurehaltiger Systeme erreicht.“ Bisherige Systeme verwendeten als Elektrolyte meist in mittelkonzentrierter Schwefelsäure gelöste Vanadium-Ionen, was nicht nur teuer sei, sondern aufgrund der hochkorrosiven Lösung zu einer begrenzten Lebensdauer der Batterie führe, so Hager. Aus diesem Grund verwendet die Redox-Flow-Batterie der Jenaer Forscher Polymere, besondere Kunststoffe, die in einer wässrigen Kochsalzlösung schwimmen.
Die Jenaer arbeiten mit dem Oldenburger Energieversorger EWE bei der Umsetzung eines Pilotprojekts zusammen: EWE möchte eine Redox-Flow-Batterie (Arbeitstitel: „Brine4power“) in einem Kavernenspeicher errichten. Für diese nach eigenen Angaben weltgrößte Batterie sollen zwei Kavernen mit je 100.000 Kubikmetern Volumen verwendet werden. Sie werden mit Wasser in Salzstöcken geflutet, wodurch die benötigte Sole praktischerweise gleich vor Ort als Nebenprodukt mit entsteht. Das System soll einmal eine Leistung von 120 Megawatt erreichen und bis zu 700 Megawattstunden speichern können. Die Effizienz bei der Strom-Rückgewinnung soll bei 70 Prozent liegen. Die prognostizierten 20.000 Ladezyklen würden selbst bei täglicher Vollentladung der Batterie zu einer Lebensdauer von weit mehr als 50 Jahren führen.
Erst überirdisch, dann unterirdisch
Das Projekt hat bereits die Laborphase verlassen, bis Ende des Jahres soll zunächst ein oberirdischer Prototyp mit einer Leistung von 10 Kilowatt in Betrieb genommen werden. Weitere Prototypen folgen in den nächsten Jahren. André Fisse, Team- und Projektleiter bei der EWE Gasspeicher GmbH, berichtet: „Im November 2017 haben wir den ersten wichtigen Teilerfolg erzielen können. Wir konnten nachweisen, dass wir mit unserer Originalsole die erforderlichen benötigten elektrochemischen und Fließeigenschaften für die Elektrolytlösung sicherstellen können. Die Redox-Flow-Batterie kann in Bezug auf Leistung und Kapazität fast unbegrenzt skaliert werden – diese werden letztlich vor allem durch die schiere Größe der Speicher und die umgewälzte Elektrolytmenge definiert. Die Polymere lassen sich recyclen, alle benötigten Komponenten können ressourcenschonend beschafft werden.“
Wenn die Prototypen – der erste hat ungefähr die Größe eines Schiffscontainers – erfolgreich laufen, will man bei EWE an einem der Standorte, voraussichtlich im ostfriesischen Jemgum, die Vollausbaustufe einläuten und zwei unterirdische Gaskavernen zur Megabatterie umbauen. André Fisse: „In Jemgum läuft auch eine 110-KV-Trasse entlang, die Offshore-Windstrom in Richtung Emsland transportiert – das wäre eine ideale Möglichkeit, diesen Speicher direkt für Erneuerbare Energie einzusetzen.“
Bis es so weit ist, werden noch einige Jahre ins Land gehen: Bei EWE rechnet man damit, Ende 2023 oder Anfang 2024 eine lauffähige Kavernenbatterie ans Netz anschließen zu können. Einstweilen bleibt also abzuwarten, welche Relevanz der Lithium-Ionen-Akku bis dahin noch haben wird.
Text: Jochen Reinecke
